Cho 3,78g hỗn hợp gồm Al và Mg vào dung dịch HCl 0,5M thu được 9,916 lít khí H2
a) tính thể tích dung dịch HCl đã phản ứng
b) tính thành phần % theo khối lượng mỗi chất có trong hợp chất ban đầu
Hòa tan 14,6g hỗn hợp gồm Zn và ZnO vào một lượng vừa đủ dung dịch HCl 0,5M thì thu được 2,24 lít khí (đktc).
a/ Tính thành phần phần trăm khối lượng mỗi chất trong hỗn hợp đầu.
b/ Tính thể tích dung dịch HCl 0,5 M đã phản ứng
nH2 = 2.24/22.4 = 0.1 (mol)
Zn + 2HCl => ZnCl2 + H2
ZnO + 2HCl => ZnCl2 + H2O
nZn = nH2 = 0.1 (mol)
=> mZn = 6.5 g
mZnO = 14.6 - 6.5 = 8.1 (g)
nZnO = 0.1 (mol)
%Zn = 6.5/14.6 * 100% = 44.52%
%ZnO = 55.48%
nHCl = 0.1*2 + 0.1*2= 0.4 (mol)
Vdd HCl = 0.4 / 0.5 = 0.8 l
Hòa tan 9,6g hỗn hợp gồm Mg và MgO vào dung dịch HCl 10,95% (vừa đủ). Sau phản ứng thu được dung dịch A và 3,36 lít khí Hiđro (đktc).
a) Tính thành phần phần trăm về khối lượng mỗi chất trong hỗn hợp ban đầu.
b) Tính khối lượng dung dịch HCl đã sử dụng
c) Tính nồng độ phần trăm dung dịch thu được
Cho 27 gam hỗn hợp A gồm Al và ZnO vào dung dịch HCl 29,2%(vừa đủ) thì thu được 13,44 lít khí H2(đktc)
a) Tính khối lượng mỗi chất trong hỗn hợp ban đầu?
b) Tính khối lượng dung dịch HCl cần dùng?
c) Tính nồn độ phần trăm các muối có trong dung dịch thu được sau phản ứng?
Cho 27 gam hỗn hợp A gồm Al và ZnO vào dung dịch HCl 29,2%(vừa đủ) thì thu được 13,44 lít khí H2(đktc)
a) Tính khối lượng mỗi chất trong hỗn hợp ban đầu?
b) Tính khối lượng dung dịch HCl cần dùng?
c) Tính nồn độ phần trăm các muối có trong dung dịch thu được sau phản ứng?
2Al + 6HCl -> 2AlCl3 + 3H2 (1)
ZnO + 2HCl -> ZnCl2 + H2O (2)
a) nH2= 13,44/22.4=0.6(mol) -> mH2=0,6.2=1,2(g)
Theo PTHH: nAl = 2/3 nH2 = 2/3 . 0,6= 0,4(mol) -> mAl = 0,4 . 27=10,8(g)
-> mZnO = 27-10,8= 16,2(g)
b) nZnO = 16,2/81=0,2(mol)
Theo PTHH (2): nHCl = 2nZnO=2.0,2=0,4(mol)
Theo PTHH (1) : nHCl=2nH2=2.0,6=1,2(mol)
-> \(\Sigma\)nHCl = 0,4+1,2=1,6(mol)
-> mHCl = 1,6.36,5= 58,4(g)
-> mddHCl = 58,4.100/29,2= 200(g)
c) Theo PTHH (1): nAlCl3 = 2/3 nH2 = 2/3 . 0,6=0,4(mol) -> mAlCl3=0,4.133,5=53,4(g)
mdd sau phản ứng= mA + mddHCl - mH2 =27+200-1,2 =225,8(g)
-> C% AlCl3 = 53,4.100%/225,8 = 20,88%
Theo PTHH (2) nZnCl2 =nZnO= 0,2(mol)-> mZnCl2=0,2.136=27,2(g)
-> C% ZnCl2= 27,2.100%/255,8=10,63%
Cho 30,7 gam hỗn hợp gồm kẽm và sắt tác dụng hoàn toàn với dung dịch HCl 2M, sau phản ứng thu được 11,2 lít khí ở đktc. a) Tính thành phần phần trăm theo khối lượng mỗi kim loại trong hỗn hợp ban đầu b) Tính thể tích dung dịch HCl đã phản ứng
a,\(n_{H_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
PTHH: Zn + 2HCl → ZnCl2 + H2
Mol: x x
PTHH: Fe + 2HCl → FeCl2 + H2
Mol: y y
Ta có: \(\left\{{}\begin{matrix}65x+56y=30,7\\x+y=0,5\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,3\left(mol\right)\\y=0,2\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\%m_{Zn}=\dfrac{0,3.65.100\%}{30,7}=63,52\%;\%m_{Fe}=100\%-63,52\%=36,48\%\)
b,
PTHH: Zn + 2HCl → ZnCl2 + H2
Mol: 0,3 0,6
PTHH: Fe + 2HCl → FeCl2 + H2
Mol: 0,2 0,4
nHCl = 0,6+0,4 = 1 (mol)
\(V_{ddHCl}=\dfrac{1}{2}=0,5\left(l\right)=500\left(ml\right)\)
Cho 13g hỗn hợp A gồm Cu, Al, Mg vào dung dịch HCl dư, phản ứng xong thu được 4 gam chất rắn không tan và 10,08 lít khí H 2 (đktc). Tính thành phần phần trăm theo khối lượng của từng kim loại trong hỗn hợp.
A. 30,77%; 27,69%; 41,54%
B. 27,69%; 41,54%; 30,77%
C. 30,77%; 41,54%; 27,69%
D. 27,69%; 30,77%;41,54%
2Al + 6HCl → 2 A l C l 3 + 3 H 2
a……….3/2.a (mol)
Mg + 2HCl → M g C l 2 + H 2
b....................b (mol)
4 gam rắn không tan là Cu, gọi số mol của Al và Mg lần lượt là a và b (mol). Ta có:
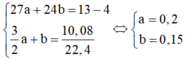
⇒ % m C u = 4 13 .100 = 30,77 % ⇒ % m A l = 0,2.27 13 .100 = 41,54 % ⇒ % m M g = 100 % − 30,77 % − 41,54 % = 27,69 %
⇒ Chọn C.
Cho 10g hỗn hợp gồm Fe và Cứ tác dụng với đang dịch HCl 0,5M. Sau phản ứng thu được 3,36l khí (đktc) và chất rắn A không tan a. Tính khối lượng Fe trong hỗn hợp ban đầu b. Tính khối lượng Cứ trong hỗn hợp ban đầu c. Tính thể tích dung dịch HCl đã tham gia phản ứng Giúp em với ạ
Vì Cu không tác dụng với HCl, nên chỉ có phản ứng của Fe.
PTHH: Fe+2HCl\(\rightarrow\)FeCl2+H2
a) nH2=0,15(mol)
Theo pt: nFe=nH2=0,15 (mol)
\(\Rightarrow\)mFe=8,4(g)
b) mCu=10-8,4=1,6(g)
c) Theo pt: nHCl=nH2=0,15(mol)
\(\Rightarrow\)VHCl=0,3(l)
Hoà tan hết 12 gam hỗn hợp gồm Fe và FeO vào dung dịch HCl vừa đủ, phản ứng xong thu được 211,7 gam dung dịch A và 3,36 lít khí H2 ở ĐKTC.
a) Tính khối lượng mỗi chất trong hỗn hợp ban đầu
b) Tính nồng độ phần trăm của dung dịch HCl đã dùng.
c) Tính nồng độ phần trăm của chất có trong dung dịch A
a,Fe + 2HCl → FeCl + H2 (1)
FeO + 2HCl → FeCl + H2O (2)
nH2 = 3,36/ 22,4 = 0,15 ( mol)
Theo (1) nH2 = nFe = 0,15 ( mol)
mFe = 0,15 x 56 = 8.4 (g)
m FeO = 12 - 8,4 = 3,6 (g)
a, \(n_{H_2}=\frac{3,36}{22,4}=0,15\left(mol\right)\)
\(Fe+2HCl->FeCl_2+H_2\left(1\right)\)
\(FeO+2HCl->FeCl_2+H_2O\left(2\right)\)
theo (1) \(n_{Fe}=n_{H_2}=0,15\left(mol\right)\)
=> \(m_{Fe}=0,15.56=8,4\left(g\right)\)
=> \(m_{FeO}=12-8,4=3,6\left(g\right)\)
Hoà tan hết 12 gam hỗn hợp gồm Fe và FeO vào dung dịch HCl vừa đủ, phản ứng xong thu được 211,7 gam dung dịch A và 3,36 lít khí H2 ở ĐKTC.
a) Tính khối lượng mỗi chất trong hỗn hợp ban đầu
b) Tính nồng độ phần trăm của dung dịch HCl đã dùng.
c) Tính nồng độ phần trăm của chất có trong dung dịch A
ta thấy : nFe =nH2 = 0,15
=> mFe =0,15 x 56 = 8,4g
%Fe=8,4/12 x 100 = 70%
=>%FeO = 100 - 70 = 30%
b) BTKLra mdd tìm mct of HCl
c) tìm mdd sau pứ -mH2 nha bạn